Халькопирит - формула, свойства
Английское название минерала халькопирит - Chalcopyrite
Название халькопирита образовано от греч. халькос — медь, пирос — огонь.
Синонимы минерала: Медный колчедан, желтая медная руда, тованит (Милер-Брук, 1852), купропирит (Узри, 1920). Измененным халькопиритом является гомихлин (Брайт- хаунт, 1858). Барнгардтит (барнхардтит; Гент, 1855) — смесь халькопирита с другими минералами.

Содержание
- Химический состав
- Кристаллографическая характеристика
- Форма нахождения в природе
- Физические свойства
- Химические свойства
- Диагностические признаки
- Происхождение
- Месторождения
- Практическое применение
- Физические методы исследования
- Кристаллооптические свойства в тонких препаратах (шлифах)
- Купить
Формула халькопирита
CuFeS2.
Химический состав
Минерал халькопирит состоит из Сu — 34,57 %, Fe — 30,54 %, S — 34,9 %. Данные химических анализов обычно очень близки к этим цифрам. В качестве примесей в ничтожных количествах иногда присутствуют Ag, Аu Tl, Se, Те.
Кристаллографическая характеристика халькопирита
Сингония тетрагональная; тетрагональноскаленоэдрический в. с. L24L22P.
Две модификация: Тетрагональный и кубический— высокотемпературная. кубический X. не гомогенен, а состоит из тонких пластинчатых и решетчатых срастаний кубический и Тетрагональный модификация X. габитус: псевдотетраэдрический, реже дипирамидальный и скаленоэдрический.
Кристаллическая структура
Структура халькопирита сходна со структурой сфалерита. Если считать Си и Fe эквивалентными, то решетка халькопирита будет точно отвечать решетке сфалерита. Тетрагональный характер решетки является результатом чередования Fe- и Cu-тетраэдров по закону четверной зеркально-поворотной оси; благодаря этому чередованию параметр по оси с по сравнению со сфалеритом оказывается удвоенным. Каждый атом S окружен четырьмя атомами металла (2Cu + 2Fe) по углам почти правильного тетраэдра; каждый атом металла окружен 4S. Расстояния Сu — S 2,32, Fe—S 2,20. Cu и Fe, по-видимому, не имеют фиксированных положений, и составу ячейки отвечает как Cu1+Fe3+S2, таки Cu2+Fe2+S2.
Главные формы:
Кристаллы халькопирита большей частью псевдотетраэдрический или псевдооктаэдрический при равном развитии положительных и отрицательных тетрагональных тетраэдров; также дипирамидальный и скаленоэдрический. Наиболее развиты обычно грани р( 112) со штриховкой || ребрам (112): (101) и (112): (102) или матовые, реже встречаются р(112) — гладкие, блестящие.
Форма нахождения в природе
Облик кристаллов. Кристаллы редки и встречаются только в друзовых пустотах.
Двойники минерала. Обычно у халькопирита наблюдаются двойники {112}, {102}, {110},. Преимущественно развиты двойники по (112) с плоскостям срастания (112) или перпендикулярной к ней (двойники срастания и прорастания, пятерники, полисинтетические двойники); реже двойники по (102) и сложные двойники прорастания с двойниковой осью [001] и плоскостью срастания (110). Тонкие полисинтетические, часто изогнутые двойники возникают при динамических воздействиях.
Известны параллельные срастания со сфалеритом и тетраэдритом (в связи со сходством структур), а также почти параллельные срастания с пиритом, кобальтином и галенитом. Часто халькопирит нарастает на тетраэдрит, а иногда тетраэдрит его обволакивает.
Агрегаты халькопирита. Зернистые массы или отдельные зерна (вкрапленности), иногда кристаллы и их группы; сравнительно редки скрытокристаллические почковидные натечные агрегаты.

Физические свойства
Оптические
- Цвет латунно-желтый неповторимого, типичного именно для халькопирита оттенка., золотисто-желтый.
- Черта у минерала черная с зеленоватым оттенком, местами металлически блестящая.
- Блеск сильный металлический.
- Отлив - нередко пестрая побежалость
- Прозрачность Непрозрачен
Механические
- Твердость 3—4.
- Плотность 4,1—4,3 (вычисл. 4,283).
- Спайность по (112) и (101) несовершенная.
- Излом раковистый до неровного.
Довольно хрупок.
Химические свойства
Халькопирит растворяется в HNO3 с выделением S. В НСl минерал не растворяется.
В полированных шлифах очень слабо травится HNO3 и KCN. Структурные особенности агрегатов хорошо выявляются при травлении парами царской водки, парами концентрированной НСl + CrOз, а также раствором KMnO4+ КОН или HNO3+ KCl3. В закрытой трубке — возгон S.
Прочие свойства
Хороший проводник электричества. Удельное сопротивление значительно снижается по мере повышения температуры.
Температура плавления минерала 1000°. Коэффициент линии расширения до 40°, в среднем 0,000017 (Ниггли). На дифференциальной кривой нагревания в атмосфере азота или углекислоты — острый эндотерм, пик с максимумом при 560° и два незначительных по величине эндотермических прогиба, связанных с переходом в другие модификации.
При высоких температурах образуется кубическая разновидность, изоструктурная со сфалеритом. При температуре выше 250° халькопирит удерживает в твердом растворе CuFe2S3 (кубанит), при понижении температуры последний обособляется.
Искусственное получение халькопирита.
Мелкие кристаллики халькопирита в форме тетрагональных тетраэдров получены действием H2S на слабо нагретую смесь 2CuO + Fe2Oз, а также при обработке сероводородной водой смеси карбоната меди и Fe2 (SO4)3 в закрытую трубку (по Дёльтеру), действием слабощелочного раствора CuCl2 на кристаллы K.2Fe2S4 (в отсутствие воздуха).
Диагностические признаки
Узнаётся по латунно-жёлтому цвету, зеленовато-чёрной черте, пёстрой побежалости, средней твёрдости (не царапает стекло).

В сплошных массах минерал похож на пирит, но обладает более желтым цветом и меньшей твердостью и отсутствием кубических кристаллов. В отличие от золота хрупок. От кубанита и миллерита отличается по форме кристаллов. Под микроскопом халькопирит настолько характерен, что его трудно спутать с другими минералами, однако в очень мелких зернах и при отсутствии возможности непосредственного сравнения с другими сульфидами может быть принят за кубанит, миллерит, пирит, золото. Кубанит более кремовый, более анизотропен; миллерит и пирит имеют и более высокую отражательную способность, первый более твердый и изотропен, второй :— сильно анизотропен и двуотражает; золото значительно ярче, обладает своеобразным блеском при скрещенных николях.
Спутники. Кварц, кальцит, сидерит, пирит, галенит, сфалерит, пирротин, пентландит, арсенопирит, магнетит, кобальтин, турмалин, энаргит, гюбнерит
Происхождение и нахождение
В природе халькопирит может образовываться в различных условиях. Встречается в различных магматогенных месторождениях скарнах в Cu-Ni, W-Mo-Sn, Pb-Zn и колчеданных месторождениях, гидротермальных зонах, известен также как минерал некоторых осадочных пород.
Как спутник пирротина он часто встречается в магматогенных месторождениях медноникелевых сульфидных руд в основных изверженных породах в ассоциации с пентландитом, магнетитом, иногда кубанитом и др.
Наиболее широко развит в типичных гидротермальных жильных и метасоматических (в том числе и контактовометасоматических) месторождениях. Он обычно ассоциирует с пиритом, пирротином, сфалеритом, галенитом, блеклыми рудами и многими другими минералами. Из нерудных минералов в этих месторождениях встречаются кварц, кальцит, барит, различные по составу силикаты и др.
При экзогенных процессах халькопирит образуется очень редко среди осадочных пород в условиях сероводородного брожения при разложении органических остатков и притоке меденосных растворов. Наблюдались явления замещения им древесины и организмов (наряду с халькозином и марказитом), в месторождениях фосфоритов.
Кубический X. обнаружен только в сульфидных Cu-Ni м-нийх, связанных с ультраосновными и основными изверженная порода
В процессе выветривания халькопирит, разрушаясь химически, дает сульфаты меди и железа. Растворимый сульфат меди при взаимодействии с CO2 или с карбонатами в присутствии кислорода и воды образует малахит и азурит; с гидрозолями SiO2 — хризоколлу; при взаимодействии с различными кислотами, образующимися в зоне выветривания, — разнообразные соли: арсенаты, фосфаты, ванадаты, иногда хлориды и др. В условиях очень сухого климата в зоне окисления сохраняются также различные сульфаты меди, легко растворимые в просачивающихся поверхностных водах.
Псевдоморфозы по халькопириту, т. е. замещение его вторичными сульфидами меди — борнитом, халькозином и ковеллином, широко распространены в зонах вторичного сульфидного обогащения медных месторождений.
Халькопирит в качестве спутника в тех или иных количествах встречается почти во всех гидротермальных месторождениях самых различных сульфидных руд. В рудах многих месторождений он является существенной составной частью и имеет самостоятельное промышленное значение. На территории России и ближнего зарубежья мы имеем представителей всех генетических типов месторождений, в которых халькопирит является главным минералом меди. В очень редких случаях медный колчедан образуется в зоне вторичного сульфидного обогащения медных месторождений.
На Урале широко распространены так называемые колчеданные залежи, приуроченные к толщам большей частью метаморфизованных эффузивно-осадочных пород палеозойского возраста. Главным минералом (до 60–80 %) в рудах этих месторождений является пирит, с которым парагенетически связан халькопирит. К этому типу относится большая часть уральских месторождений. В некоторых залежах халькопирит тесно ассоциирует со сфалеритом.
Изменение халькопирита
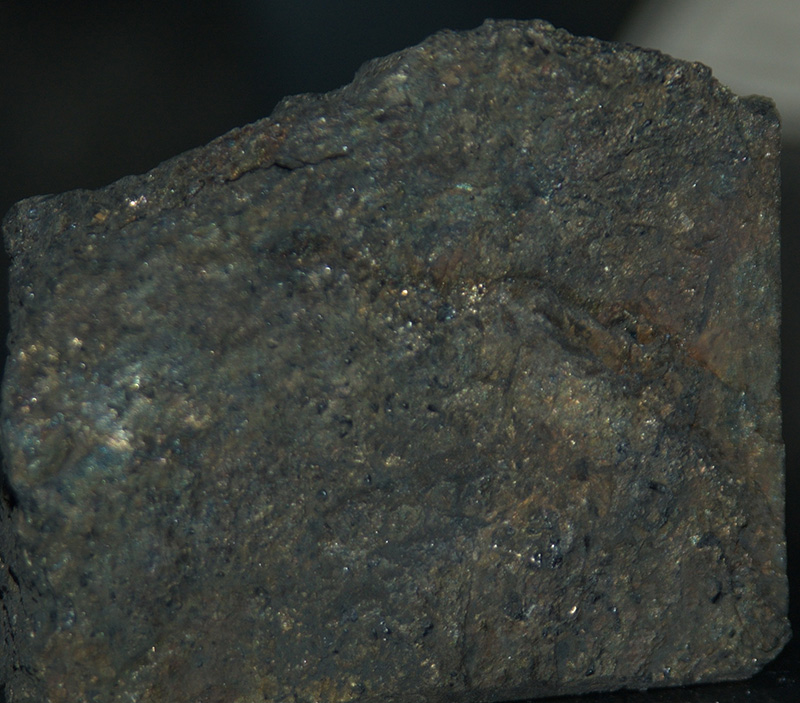
Месторождения
В наиболее высокотемпературных месторождениях, связанных с основными или ультраосновными породами, встречается либо в ассоциации с пирротином и пентландитом— Мончетундра (Мурманская обл.), Садбери (Канада), Рингерик (Норвегия), либо в ассоциации с борнитом во вкрапленных медных рудах в габбро — Волковское месторождение (Свердловская обл.)
Наиболее высокотемпературными жильными месторождениями, в рудах которых встречается медный колчедан , являются некоторые месторождения вольфрамовой и молибденовой формаций; таковы, например, месторождения Караоба, Восточный Коунрад, Северный Коунрад в Казахстане. В кварцевых жилах Корнуэлла (Англия) халькопирит наблюдается в ассоциации с касситеритом.
В месторождениях типа колчеданных залежей халькопирит наблюдается главным образом в ассоциации с пиритом, сфалеритом, отчасти с блеклой рудой, галенитом, из нерудных— с кварцем, баритом, кальцитом; таковы месторождения: им. III Интернационала, Лёвиха, Карпушинское и Дегтярское (Свердловская обл.), Блява и Яман-Касы (Оренбургская обл.), Сибай (Россия) и др. на Урале, Рио-Тинто в Испании, Бор в Сербии.
Свинцово-цинковые и медно-цинковые месторождения, в рудах которых содержится халькопирит, наряду с галенитом, сфалеритом, пиритом и другими минералами, многочисленны в Казахстане на Рудном Алтае (Белоусовское, Зыряновское, Риддерское, Заводинское и др.).
В месторождениях типа медистых песчаников халькопирит является главным минералом, но обычно тесно ассоциируется с борнитом, халькозином, блеклой рудой (месторождения этого типа]одними исследователями относятся к гидротермальным, другими — к осадочным). Крупнейшим представителем месторождений типа медистых песчаников в мире является Джезказган (Казахстан); того же типа богатейшие месторождения имеются на территории Бельгийского Конго (Катанга) и Северной Родезии.
В месторождениях вкрапленных и вкрапленно-прожилковых медных руд, связанных с кислыми) изверженными породами, халькопирит ассоциируется с пиритом, отчасти с энаргитом, блеклой рудой, молибденитом. К крупнейшим месторождениям этого типа относятся Коунрад (Казахстан), Алмалык (Узбекистан), Бингем (шт. Юта, США).
Нахождение медного колчедана в осадочных отложениях различного возраста отмечено в различных районах. Образование халькопирита в осадочных породах связывается с сероводородным брожением; в некоторых случаях вместе с ним обнаруживаются органические остатки. Медный колчедан обнаружен в девонских отложениях Татарстана (в известняках, алевролитах, аргиллитах) в ассоциации с пиритом, сфалеритом, кварцем в тонких трещинках и порах. Установлено наличие халькопирита в силурийских фосфоритах Подолии (Украина).
Практическое применение
Самый распространенный сульфид меди и главный медный минерал большинства медных руд. Халькопиритсодержащие руды являются одним из главных источников меди. Промышленное содержание ее в та ких рудах обычно колеблется в пределах 2–2,5 %.
Получаемая на металлургических заводах медь употребляется как в чистом виде, так и в виде сплавов (латуни, бронзы, томпака и др.). Главным потребителем меди является электропромышленность. Значительное количество ее расходуется в машиностроении, судостроении, изготовлении аппаратуры для химической промышленности, жилищном строительстве и т. д.
Физические методы исследования
Старинные методы. Под паяльной трубкой растрескиваясь, сплавляется в магнитный королек. На угле с содой дает королек Cu.
Кристаллооптические свойства в тонких препаратах (шлифах)
В полированных шлифах в отраженном свете желтый. Отражательная способность (в %): для зеленых лучей 41,5, для оранжевых — 40,5, для красных — 40. Двуотражение незаметно. Обладает слабой анизотропией с цветным эффектом. В зернистых агрегатах при скрещенных николях или путем структурного травления обычно обнаруживается полисинтетическое двойникование отдельных зерен.





